Novo Medicamento Para Tratamento de Alzheimer – Aducanumab Aduhelm
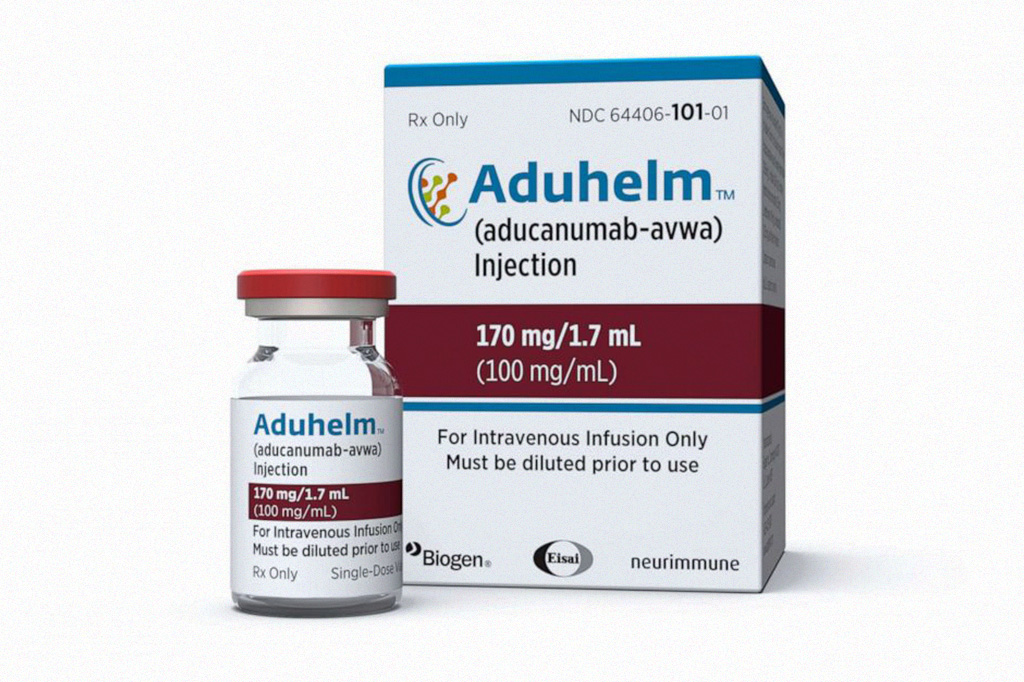
Novo Medicamento Para Tratamento de Alzheimer – Aducanumab Aduhelm: O novo medicamento para o tratamento da Doença de Alzheimer alega retardar a evolução da doença, pois vai atuar sobre mecanismos básicos dela. Esse medicamento foi liberado no dia 07 de Junho de 2021, pelo FDA, através de uma liberação acelerada.
- Aprovação FDA
- O que é o medicamento
- Como ele funciona
- Qual é a eficácia do medicamento
- Para quem ele é indicado
- Como foram os estudos para aprovação
- Negativa de Novembro 2020
- Porque e como foi aprovado junho 2021
- Quanto custo o tratamento e disponibilidade
- É ou não é uma esperança?
- Importância do diagnóstico precoce e da prevenção
Aprovação FDA – Aducanumab Aduhelm
Isso é parecido com a liberação precoce ou emergencial como a das vacinas para COVID-19, que ainda não têm vários estudos prontos, mas já recebe aprovação emergencial devido à gravidade da doença e à relevância para a sociedade. A mesma gravidade e relevância acontece com o Alzheimer. Esse novo medicamento Adalimumabe é um anticorpo monoclonal contra as placas amiloides do cérebro.
Na Doença de Alzheimer, ocorre uma deposição anormal de placas amiloides, que são uma característica típica dessa doença. E foi visto que têm pessoas que ainda não desenvolveram os sintomas clínicos francos da Doença de Alzheimer, mas anticorpos contra essas placas.
Com base nisso, foi desenvolvido um anticorpo monoclonal sintético, em que todos são clones e iguais contra essas placas amiloides. A tentativa é de limpar, tirar as placas do cérebro e com isso, possivelmente, retardar a evolução da Doença de Alzheimer.
Esse medicamento é aplicado por via endovenosa a cada quatro semanas e vai sendo aplicado indefinidamente, pois, em tese, tem que continuamente tentar retirar essas placas beta-amiloides que estão sendo formadas.
A eficácia desse medicamento foi vista fundamentalmente através dos testes laboratoriais de PET neurológico com marcadores para as placas de beta-amiloide e assim foi comparando as pessoas que receberam o medicamento versus as que receberam placebo.
As pessoas que receberam medicamentos tiveram imagens no PET com uma menor quantidade de placas amiloides em relação àquelas que receberam placebo; isso é uma evidência laboratorial. A evidência clínica também não ficou muito bem definida: parece que a melhor eficácia está no marcador laboratorial do que propriamente na clínica.
Foram 02 estudos os principais fornecedores de dados: o EMERGE e o ENGAGE. Um foi positivo, o EMERGE: apenas com doses altas e em pacientes de sintomas iniciais. Mostrou-se a redução de cerca de 20% na taxa de progressão clínica, através de testes do CDR, do mini mental e do ADAS-cog-13.
No outro estudo, o ENGAGE, não mostrou-se evidência de benefício clínico, tanto em baixas doses, como em altas doses. Em ambos os estudos, houve a redução de placas beta-amiloide.
Não foi a primeira vez que esse medicamento tentou ser aprovado. Ele já existe há mais tempo e está tentando ser aprovado desde 2015. Eles viram que é para pacientes em fase ultra precoce do Alzheimer, ou seja, não é para o paciente que normalmente chega no consultório do neurologista quando os familiares já se deram conta – e isso normalmente é em uma fase moderada da doença. Para o medicamento funcionar, tem que ser em uma fase precoce e aparentemente quanto mais precoce a fase, melhor.
Além de tudo isso, tem características que eles estão estudando que podem influenciar talvez na eficácia, como: se a pessoa tem ou não a genética da Apo-E4, que é um gene que propicia a formação de placas amiloides, e até mesmo se existem outras características que também influenciam na resposta ao medicamento.
A indicação desse medicamento não é para quem já está com a perda da memória franca e não é para quem já está com a definição muito clara da Doença de Alzheimer. É para aquela pessoa que está em estágio super inicial da doença, como foi feito nos estudos da aprovação deste medicamento.
Os estudos começaram em 2015, quando já tiveram as primeiras negativas. Depois, continuaram com um acompanhamento mais prolongado, em que fizeram com grupos mais selecionados – grupos de dose mais baixa e de dose mais alta – e fizeram acompanhamento com o estudo do mini mental, o CDR, que é uma escala de classificação clínica do Alzheimer, e também com os estudos laboratoriais do PET beta-amiloide.
Em uma primeira avaliação, não se mostrou evidência suficiente para ter aprovação dele e foi negado em Novembro de 2020. Mas, quando o laboratório fez um estudo com subgrupos muito mais selecionados, com pacientes que tinham uma clínica muito precoce e que receberam doses mais altas, foi que realmente conseguiram mostrar essa pequena melhora, que é em torno de 20% em relação ao grupo de placebo.
Esse sucesso foi obtido após 78 semanas de acompanhamento, ou seja, as pessoas tiveram que receber o medicamento a cada quatro semanas, por 78 semanas seguidas; mais de um ano para mostrar essa possível melhora e que nos exames é melhor do que aparentemente é na clínica.
Aducanumab
O Aducanumab (Aduhelm) é um medicamento que nos Estados Unidos, nessa fase inicial, ainda custa bem caro, em torno de R$50.000 por ano o tratamento, enquanto sairia no Brasil por mais de R$250.000 por ano um tratamento desse. Super vale a pena se tivesse um efeito super maravilhoso e com patamares de evidência científica muito bem definidos.
A liberação de Aducanumab foi muito debatida, pois muitos cientistas e grupos independentes não acharam que tem evidência suficiente para suportar a aprovação dele pelo FDA.
Mas teve uma outra argumentação: o FDA tem os critérios de aprovação emergencial, que é um estudo randomizado controlado com placebo, muito bem feito, e mais outra evidência de suporte para a aprovação.
Com esses dois elementos que teve com esse estudo de subgrupo e os estudos que vieram positivos no PET-amiloide, eles aprovaram para a liberação emergencial, pela argumentação de que a Doença de Alzheimer é uma doença grave e muito relevante para a sociedade. O Alzheimer é uma doença massificada, especialmente, nos países desenvolvidos, tanto que é um problema de saúde pública
Efeitos Colaterais
Os efeitos colaterais e os possíveis problemas relacionados ao medicamento são poucos, ou seja, ele tem um bom perfil de segurança. Os possíveis efeitos colaterais estão relacionados a qualquer medicamento biológico de infusão, que basicamente seriam: dor de cabeça; um certo mal estar no corpo; no dia da infusão, alergias e assim por diante.
São efeitos colaterais menores que, de maneira geral, são bem tolerados e ainda assim vale a pena a aprovação, condicionado a ainda fazer um novo estudo para verificar se confirma ou não essa provação de agora, ou seja, a provação ainda é uma provação limitada.
Ela está condicionada a uma nova aprovação, a um novo estudo posterior que seja mais amplo, que tenha um maior número de pessoas com doses maiores e precoces para ver se sustenta realmente o benefício dele comparado com placebo e dele mesmo comparado com medicamentos e terapêuticas já convencionais em relação ao Alzheimer.
No final das contas, isso é uma esperança ou não? É sim, é uma esperança, mas não esperança de que mesmo nos seus melhores resultados, não é de um resultado tão grande, é de um resultado razoavelmente modesto.
Mas com a somatória de terapêuticas, como a de um medicamento que reduz 20%, um suplemento que reduz 10%, a atividade física, a alimentação saudável, é possível somar elementos protetores. E com essa somatória de terapêuticas é possível ter um volume muito maior de prevenção.
Então fica a pergunta, o Aducanumab é ou não uma esperança? É sim uma esperança, mas não é uma esperança de cura. É uma esperança de um retardo relativamente modesto da evolução da doença e que ainda necessita ser comprovada e ratificada de uma maneira mais poderosa, através de mais evidências científicas de eficácia terapêutica.
Mais importante de tudo isso e desse estudo é que, aparentemente, qualquer terapêutica que venha a funcionar para a Doença de Alzheimer só vai funcionar se for aplicada em estágios ultra precoces da doença.
Necessita-se de uma forma de diagnóstico precoce, de uma rotina de investigação e de rastreio de doenças do cérebro, de um check-up neurológico, para que os diagnósticos sejam realizados precocemente ou até mesmo para que seja possível aplicar as terapêuticas que possam, por ventura, ser desenvolvidas.
Fazer os elementos de prevenção que nós já conhecemos, como hábitos saudáveis; dormir bem; atividade física, que é fenomenal; alimentação saudável e rica em boas gorduras, como a alimentação mediterrânea. E, fundamentalmente, só vai haver esperança para aquelas pessoas que tiverem essa capacidade de ter um diagnóstico precoce e de fazer a terapêutica precocemente.
Lógico que em um futuro breve o custo desse tratamento vai cair, mas neste momento, o medicamento está disponível nos Estados Unidos apenas e a aprovação é apenas lá.
E para um medicamento biológico, como o Aducanumab, é difícil de pensar que alguém vai ficar importando mensalmente um estoque para trazer aqui para o Brasil. Então, podemos ter esperança de um possível novo medicamento, que ainda é restrito para populações muito bem selecionadas e extremamente caro, de mais uma arma para combatermos essa doença tão terrível que é a Doença de Alzheimer.
- https://www.fda.gov/drugs/news-events-human-drugs/fdas-decision-approve-new-treatment-alzheimers-disease
- https://www.fda.gov/news-events/press-announcements/fda-grants-accelerated-approval-alzheimers-drug
- https://www.tandfonline.com/doi/full/10.1586/17512433.2015.1034690
- https://www.thelancet.com/journals/laneur/article/PIIS1474-4422(19)30480-6/fulltext
- https://alz-journals.onlinelibrary.wiley.com/doi/10.1002/alz.12213